Nghe nồng độ đương lượng khá là giống với nồng độ Molan – nhưng thực tế chúng có liên quan hay giống nhau hay không? Chúng ta hãy cùng sieutonghop.com tìm hiểu nhé.
1. Nồng độ đương lượng là gì?
Nồng độ đương lượng (gọi là nồng độ đương lượng gam) là đơn vị đo lường dùng được dùng trong hóa học và sinh học. Đương lượng dùng để đo lường khả năng một chất kết hợp với các chất khác. Đương lương thường được dùng khi nói về nồng độ chuẩn.
– Biểu thị số đượng lượng gam chất tan chứa trong 1l dung dịch, kí hiệu N.
– Ví dụ: dung dịch NaCl 1N là dung dịch mà trong 1l của nó có chứa 1 đương lượng gam
NaCl, tức 58.5g; Dung dịch H2SO4 1N là dung dịch mà trong 1l của nó có chứa 1 đương
lượng gam H2SO4, tức 49g.
2. Cách tính nồng độ đương lượng?
Bạn có thể tính nồng độ đương lượng qua công thức sau:
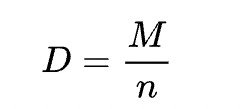
Trong đó:
- D là đương lượng gram
- n là số mol
- M là khối lượng
Cách để xác định n là:
- Nếu là axit thì n là số H+ có trong phân tử axit
- Nếu là bazơ thì n là số nhóm OH- có trong phân tử bazơ
- Nếu là muối thì n bằng tổng số hóa trị của các nguyên tử kim loại có trong muối.
- Nếu là chất oxi hóa hoặc chất khử thì n là số electron nhận hay cho của chất đó
Công thức tính nồng độ đương lượng CN: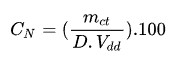
Trong đó:
- Mm chất tan là khối lượng chất tan nguyên chất (gram)
- D là đương lượng gram của chất
- Vdd là thể tích dung dịch (ml)
- CN là nồng độ đương lượng của dung dịch N nào đó.
3. Bài tập nồng độ đương lượng có lời giải?
Ví dụ 1:
Bạn có một dung dịch muối natri (NaCl) với nồng độ 0.5 mol/L. Hãy tính khối lượng muối cần phải sử dụng để làm 500 mL dung dịch này.
Giải:
– Sử dụng công thức nồng độ đương lượng (C) để tính số mol muối:![]() – Sử dụng số mol để tính khối lượng muối sử dụng công thức: Khối lượng (g)= Số mol x khối lượng molar
– Sử dụng số mol để tính khối lượng muối sử dụng công thức: Khối lượng (g)= Số mol x khối lượng molar
– Trong trường hợp này, khối lượng molar của muối natri (NaCl) là khoảng 58.44 g/mol.
Lời giải chi tiết:
- Số mol muối (NaCl) = 0.5 mol/L×0.5 L=0.25 mol
- Khối lượng muối (NaCl) = 0.25 mol×58.44 g/mol=14.61
Vì vậy, để làm 500 mL dung dịch muối natri có nồng độ 0.5 mol/L, bạn cần sử dụng khoảng 14.61 gram muối natri.
Ví dụ 2:
Bạn có một dung dịch axit sulfuric () với nồng độ 2.0 mol/L. Hãy tính khối lượng axit cần để làm 250 mL dung dịch này.
Sử dụng công thức nồng độ đương lượng để tính số mol axit sulfuric:![]() Sử dụng số mol để tính khối lượng axit sử dụng khối lượng molar của axit sulfuric (), với khối lượng molar khoảng 98 g/mol.
Sử dụng số mol để tính khối lượng axit sử dụng khối lượng molar của axit sulfuric (), với khối lượng molar khoảng 98 g/mol.
Lời giải chi tiết:
- Số mol axit sulfuric () = 2.0 mol/L×0.25 L=0.5 mol
- Khối lượng axit sulfuric () = 0.5 mol×98 g/mol=49 g
Vậy nếu bạn muốn làm 250 mL dung dịch axit sulfuric có nồng độ 2.0 mol/L, bạn cần sử dụng 49 gram axit sulfuric