Trong cấp 2 cụ thể là ở lớp 8 chúng ta đã được học về nguyên tử là gì rồi? Và bài viết này mình sẽ cùng các bạn tìm hiểu chi tiết về Nguyên tử là gì cùng cấu tạo của hạt nguyên tử nhé!
1. Nguyên tử là gì?
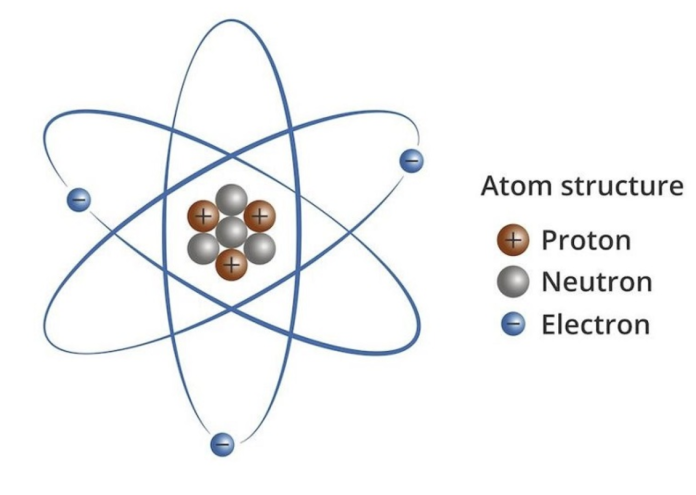
 Nguyên tử là hạt vô cùng nhỏ, trung hòa về điện và là thành phần cơ bản cấu tạo nên các chất. Nguyên tử bao gồm một hạt nhân mang điện tích dương ở giữa, xung quanh là các electron mang điện tích âm chuyển động theo quỹ đạo.
Nguyên tử là hạt vô cùng nhỏ, trung hòa về điện và là thành phần cơ bản cấu tạo nên các chất. Nguyên tử bao gồm một hạt nhân mang điện tích dương ở giữa, xung quanh là các electron mang điện tích âm chuyển động theo quỹ đạo.Sách giáo khoa Hóa học 8 (Nhà xuất bản Giáo dục Việt Nam) định nghĩa về nguyên tử như sau: “Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện. Nguyên tử gồm hạt nhân mang điện tích dương và vỏ tạo bởi một hay nhiều electron mang điện tích âm”.
Electron ký hiệu là e có điện tích âm nhỏ nhất và được quy ước ghi bằng dấu âm (-).
2. Cấu tạo của hạt nguyên tử?
Hạt nguyên tử gồm 3 phần chính đó là:
- Electron: Các hạt mang điện tích âm, chuyển động xung quanh hạt nhân trong các quỹ đạo.
- Proton: Các hạt mang điện tích dương, nằm trong hạt nhân.
- Neutron: Các hạt không mang điện, cũng nằm trong hạt nhân.
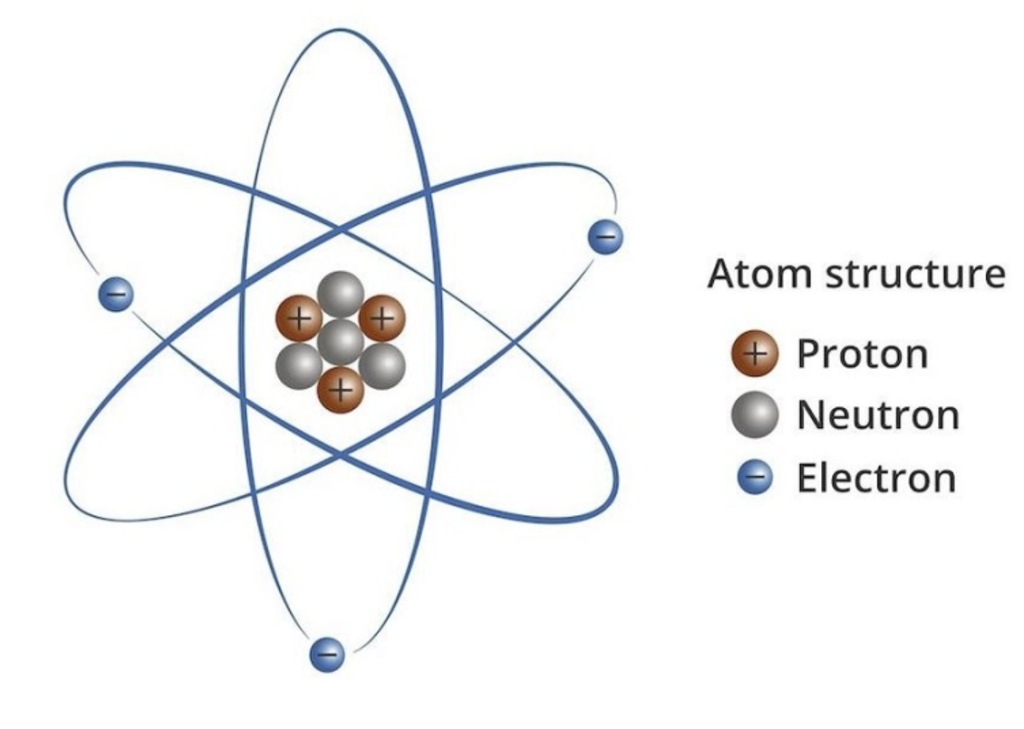
Cụ thể:
Electron:
- Khối lượng Electron: ~9.109 × 10⁻³¹ kg (rất nhỏ, chỉ khoảng 1/1836 khối lượng của proton).
- Điện tích: -1.602 × 10⁻¹⁹ Coulomb.
- Kích thước: Bán kính của electron khoảng 2.817 × 10⁻¹⁵ mét.
Proton:
- Khối lượng Proton: ~1.673 × 10⁻²⁷ kg.
- Điện tích: +1.602 × 10⁻¹⁹ Coulomb (điện tích dương bằng với giá trị tuyệt đối của electron).
- Kích thước: Bán kính khoảng 0.84 – 0.87 femto mét (1 femto mét = 10⁻¹⁵ mét).
Neutron:
- Khối lượng Neutron: ~1.675 × 10⁻²⁷ kg (hơn proton một chút).
- Điện tích: 0 Coulomb (không mang điện tích).
- Kích thước: Tương tự proton, khoảng 0.84 – 0.87 femto mét.
Kích thước nguyên tử ảnh hưởng đến tính chất của vật chất, ví dụ như điểm nóng chảy và khả năng phản ứng hóa học.
3. Các định nghĩa khác liên quan đến nguyên tử?
– Hạt nhân nguyên tử:
Hạt nhân nguyên tử được cấu tạo từ proton và neutron, còn electron chuyển động bên ngoài hạt nhân, tạo nên cấu trúc tổng thể của nguyên tử. Proton ký hiệu là p và có điện tích như electron nhưng khác dấu (ghi bằng dấu dương +). Nơtron không mang điện, ký hiệu là n. Các nguyên tử cùng loại đều có số proton trong hạt nhân.
– Số nguyên tử là gì?
Số nguyên tử là số lượng proton được tìm thấy trong hạt nhân nguyên tử của nguyên tố hóa học đó. Trong trường hợp nguyên tử đó không có điện tích thì số lượng nguyên tử bằng số electron.
– Phân biệt nguyên tử và phân tử:
| Tiêu chí | Nguyên tử | Phân tử |
|---|---|---|
| Định nghĩa | Đơn vị nhỏ nhất của một nguyên tố hóa học | Nhóm nguyên tử liên kết với nhau qua liên kết hóa học |
| Kích thước | Rất nhỏ (khoảng 1 × 10-10 mét) | Lớn hơn nguyên tử, kích thước phụ thuộc vào số lượng và loại nguyên tử |
| Ví dụ | Nguyên tử hydro (H), carbon (C), oxi (O) | Phân tử nước (H₂O), khí oxy (O₂), carbon dioxide (CO₂) |
| Cấu trúc | Bao gồm hạt nhân (proton và neutron) và electron | Có thể bao gồm cùng một loại nguyên tử (như O₂) hoặc khác loại (như H₂O) |
| Tính chất | Có tính chất riêng của nguyên tố (ví dụ, tính kim loại hay phi kim) | Tính chất hóa học và vật lý phụ thuộc vào cách liên kết và cấu trúc phân tử |
| Tính ổn định | Có thể tồn tại độc lập nhưng không phải lúc nào cũng ổn định | Thường ổn định hơn do sự liên kết giữa các nguyên tử |
4. Bài tập ví dụ về nguyên tử?
Ví dụ 1: Câu hỏi: Nguyên tử là gì?
A) Phân tử nhỏ nhất của một hợp chất hóa học.
B) Đơn vị cơ bản của một nguyên tố hóa học.
C) Một loại hạt mang điện tích âm.
D) Một nhóm các nguyên tử liên kết với nhau.
Đáp án đúng: B) Đơn vị cơ bản của một nguyên tố hóa học.
Ví dụ 2: Các Thành Phần Của Nguyên Tử
Câu hỏi: Những thành phần nào cấu tạo nên một nguyên tử?
A) Chỉ có proton và electron.
B) Proton, neutron và electron.
C) Chỉ có neutron và electron.
D) Chỉ có proton và neutron.
Đáp án đúng: B) Proton, neutron và electron.
Ví dụ 3: Phân Biệt Nguyên Tố và Phân Tử
Câu hỏi: Sự khác biệt giữa nguyên tố và phân tử là gì?
A) Nguyên tố gồm nhiều nguyên tử, còn phân tử chỉ là một nguyên tử.
B) Nguyên tố là một loại hạt, còn phân tử là nhóm hạt liên kết với nhau.
C) Nguyên tố không thể bị phân hủy, còn phân tử có thể bị phân hủy.
D) Nguyên tố luôn là kim loại, còn phân tử luôn là phi kim.
Đáp án đúng: C) Nguyên tố không thể bị phân hủy, còn phân tử có thể bị phân hủy.
5. FaQ:
– 12 là nguyên tử khối của chất nào?
Nguyên tử khối 12 thuộc về nguyên tố Cacbon (ký hiệu hóa học là C).
– 24 là nguyên tử khối của chất nào?
Nguyên tử khối 24 thuộc về nguyên tố Crom (ký hiệu hóa học là Cr).
– Nguyên tử khối 20 là chất gì?
Nguyên tử khối 20 thuộc về nguyên tố Canxi (ký hiệu hóa học là Ca).
– Nguyên tử khối 14 là nguyên tố nào?
Nguyên tử khối 14 thuộc về nguyên tố Silic (ký hiệu hóa học là Si).
– 32 là nguyên tử khối của nguyên tố nào?
Nguyên tử khối 28 thuộc về nguyên tố Niken (ký hiệu hóa học là Ni).
– 48 là nguyên tử khối của nguyên tố nào?
Nguyên tử khối 48 thuộc về nguyên tố Cadimi (ký hiệu hóa học là Cd).
– Nguyên tử khối 27 là chất gì?
Nguyên tử khối 27 thuộc về nguyên tố Nhôm (ký hiệu hóa học là Al).
– 56 là nguyên tử khối của nguyên tố nào?
Nguyên tử khối 56 thường được liên kết với nguyên tố sắt (Fe). Sắt có số hiệu nguyên tử là 26 và là một trong những kim loại quan trọng trong hóa học và công nghiệp.
– Nguyên tử khối 18 là chất gì?
Nguyên tử khối 18 thuộc về nguyên tố Argon (ký hiệu hóa học là Ar), một khí hiếm trong nhóm khí trơ.
> êlectron là gì? Cấu tạo của các hạt nguyên tử




















[…] Nguyên tử là gì? Cấu tạo của hạt nguyên tử […]
Comments are closed.